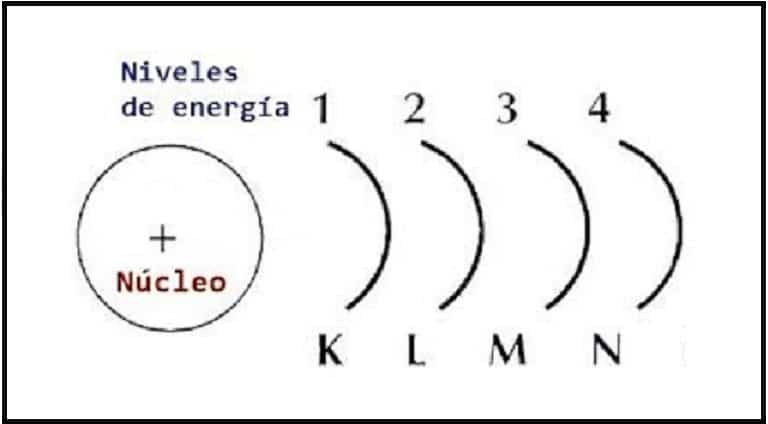
.Un sistema o partícula de la mecánica cuántica que está ligado, es decir, confinado espacialmente. Solo puede tomar ciertos valores discretos de energía, citados niveles de energia.
Esto contrasta con las partículas clásicas, que logran tener cualquier cantidad de energía. El vocablo se usa usualmente para los niveles de energía de los electrones en átomos, iones o moléculas, que existen unidos por el campo eléctrico del núcleo. Asimismo pueden referirse a niveles de energia de núcleos o vibraciones o niveles de energía rotacional en moléculas. Se dice que el espectro de energía de un sistema con niveles de energia tan discretos está medido.
En química y física atómica
En química y física atómica, una capa de electrones, o nivel de energía primordial, puede reflexionar como la órbita de uno o más electrones cerca del núcleo de un átomo.
Las capas del nucleo tienen el siguiente nombre:
- La capa más cercana al núcleo se llama » 1 capa» (también llamada «capa K»)
- La segunda » 2 capa» (o «capa L»)
- Despues la » 3 capa» (o «capa M»).
Las capas se pertenecen con los principales números cuánticos (n=1,2,3,4) o están etiquetados alfabéticamente con letras traídas en la notación de rayos X (K, L, M, N…).
Cada capa puede sujetar solo un número fijo de electrones: la primera capa puede sujetar hasta dos electrones, la segunda capa puede sujetar hasta ocho (2+6) electrones, la tercera capa puede contener hasta 18 (2+6+10) etc. La fórmula general es que la capa n-esima puede, en primicia, contener hasta 2 (n 2) electrones.
Dado que los electrones son atraídos eléctricamente al núcleo, los electrones de un átomo generalmente ocuparán las capas externas solo si las capas más internas ya se han llenado por perfecto con otros electrones. Sin embargo, este no es una exigencia estricto: los átomos pueden tener dos o incluso tres capas externas incompletas. Para obtener una ilustración de por qué existen electrones en estas capas, consulte la configuración de electrones.
La energía potencial se instaura en cero a una distancia infinita del núcleo o molécula atómica, la convención habitual. Los estados de electrones atados tienen energía potencial negativa.
Niveles de energia de un átomo, ión o molécula
Un átomo, ión o molécula se halla en el nivel de energía más bajo posible, se dice que él y sus electrones están en el estado esencial. Si se está en un nivel de energía más alto, se dice que ser excitado, o cualquier electrones que poseen mayor energía que el estado esencial son excitados.
Si más de un estado de la mecánica cuántica tiene la misma energía, los niveles de energía están «degenerados». Luego se designan niveles de energía degenerados.
Los niveles de energia medidos resultan de la conducta ondulatorio de las partículas, lo que da una relación entre la energía de una partícula y su longitud de onda.
Para una partícula confinada, como un electrón en un átomo, los puestos de onda que tienen energías bien determinadas tienen la forma de una onda estacionaria. Los estados que tienen energías bien definidas se nombran estados estacionarios porque son los estados que no cambian en el tiempo.
De modo informal, estos estados incumben a un número entero de longitudes de onda de la función de onda lo largo de una ruta cerrada (una ruta que termina donde comenzó). Es igual que una órbita circular cerca de un átomo, donde el número de longitudes de onda da el tipo de orbital atómico (0 para orbitales s, 1 para orbitales p, etc.).